Het succes van virale vectoren om een moleculaire lading in een cel te brengen of defecte genen te vervangen door functionele, is een keerpunt in de toekomst van de moderne geneeskunde.
Vectorproductie is een volledige workflow, inclusief :
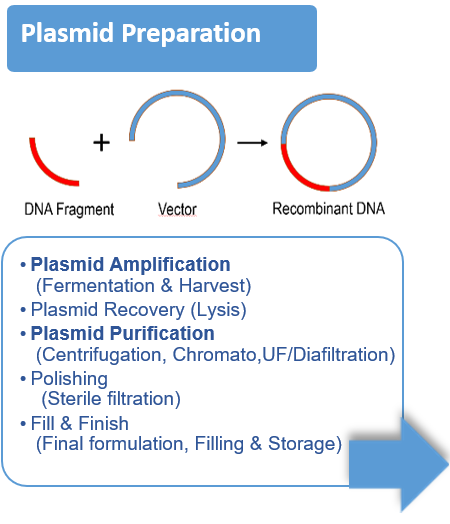
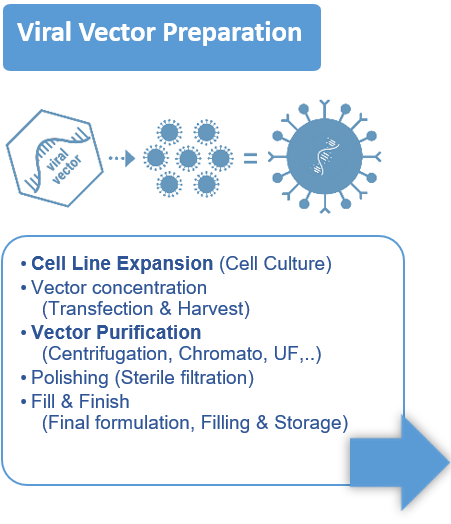
- Vectorontwerp, celuitbreiding, transfectie / infectie, cellyse, oogst / klaring, concentratie, capture, polijsten, formulering, steriele filtratie.
- Meestal is de vector een virus (AAV, Lentivirus, ..), een plasmide, maar het kan ook een Extracellulaire Vesikel of een nanopartikel zoals LNP zijn.


Uw uitdagingen in vectorproductie
- Virus- of pathogenenmanipulaties in veilige omstandigheden?
- Is uw Capsid Load-karakterisatiemethode robuust, betrouwbaar en gevalideerd?
- Hoe kan de zuiverheid van de vector worden verhoogd?
- Is uw methode voor celtelling en levensvatbaarheidsanalyse eenvoudig en betrouwbaar?
Vraag het onze experts
Onze oplossingen voor uw vectorworkflow
- Luchtbemonstering voor bewaking van levensvatbare deeltjes in cleanrooms
- Automatische vloeistofverwerking, automatische contactloze vloeistofbehandeling
- Biomassa door spectrofotometrie
- Bioreactor
- Geautomatiseerd cel telapparaten & levensvatbaarheidsanalysers
- Gezondheid van bioreactor media bioanalyzer
- Bioveiligheidskast
- Capillaire elektroforese (CE) voor plasmidezuiverheid, analyse van virale eiwitten, kwantificering van lege/volledige capsiden, genoomintegriteit
- Oogsten van cellen
- Centrifuges,centrifuge Biosafe labware en accessoires
- CO2-incubator, Shakerincubator
- Desinfectie
- Manuele Elisa-methoden met microtiterplaatlezer en microtiterplaatwasser
- Elisa Geautomatiseerde oplossingen, 10 dingen om te overwegen voor ELISA-automatisering
- Flowcytometer
- Koelkasten, vriezers en diepvriezers +4 °C tot -80 °C
- Liquid N2 Cryogene conservering
- Beeldvorming voor Western blot
- Incubator schudder
- PCR-opstelling, PCR-kast
- Pipet
- Voorbereidende ultracentrifuge, analytische ultracentrifuge (AUC)
- Viraal Vector Capside Lading door Analytische Ultracentrifugatie (AUC) of door capillaire elektroforese (CE)
- Afmeting, vorm en structuur van de virale vector door Analytische Ultracentrifugatie (AUC) door capillaire elektroforese (CE) of door Laserdiffractie (LS)
- Stoomsterilisatie
-
Waterbad
Als snelle samenvatting houdt gentherapie doorgaans in dat genetisch materiaal in cellen wordt ingebracht via een onschadelijke virale vector die de cel "infecteert" en de genetische lading aflevert. Analytische methoden zijn nodig voor het testen van grondstoffen, procescontrole en voor het aantonen van de kwaliteit van de partij virale vector. GMP-virale vectorpartijen die voor klinische proeven worden vervaardigd, moeten voldoen aan een toenemend aantal wereldwijde regelgeving. Veiligheid, identiteit, sterkte, zuiverheid en kwaliteit zijn enkele van de items die moeten worden aangetoond.
Een van de meest populaire vectoren voor verpakking is het adeno-geassocieerde virus (AAV), dat twee belangrijke voordelen heeft: efficiëntie als genleveringsvector en lage pathogeniciteit. Het virus is gemodificeerd van het wilde type om de efficiëntie als therapeutische gendrager te optimaliseren en het potentieel om ziekte te veroorzaken te minimaliseren. Recombinant AAV is vandaag de dag het leidende platform voor gentherapie.
Veilige producten creëren die op schaal kunnen worden geproduceerd – en hun veiligheid behouden – is essentieel. Het belangrijke element bij de productie van gentherapieproducten is zuiverheid, wat verwijst naar de efficiëntie van de "verpakking" voor levering in de cel. Slechte verpakking kan leiden tot minder effectieve therapie. En het toedienen van hogere doses therapie om slechte verpakking te compenseren, brengt het risico met zich mee dat er een allergische reactie bij de patiënt optreedt. De FDA heeft uitgegeven
richtlijnen
voor klinische proeven die het belang van deze kwestie benadrukken.
Alle hierboven ontwikkelde principes worden natuurlijk ook gebruikt in veel andere geavanceerde therapiegeneesmiddelen (ATMP's) dan immunotherapieën. Het is ook belangrijk te benadrukken dat, na de COVID-19-periode, de lipide nanodeeltjes (LNP's) een gebruikelijker drager zijn voor genetisch materiaal zoals mRNA.
Ontwikkeling & Productie van Virale Vectoren:
Vooruitgang in processen en vertaling voor humane gentherapie
Begrijp de rol die virale vectoren spelen in modern genonderzoek en hoe ultracentrifugatie wordt gebruikt om deze belangrijke afgiftesystemen te produceren.
Christine Le Bec - Analytical methods to measure empty & full AAV particles
Bespreking van biofysische karakteriseringstechnieken en een focus op het gebruik van analytische ultracentrifugatie (AUC) voor het meten van lege en volle AAV-deeltjes.
CRISPR voor immunotherapie: Inleiding & Overzicht
Uitgelichte video over de introductie van CRISPR voor immunotherapie.
Bronnen en referenties:
Hacein-Bey-Abina, S., Hauer, J., Lim, A., Picard, C., Wang, G. P., Berry, C. C., Martinache, C., Rieux-Laucat, F., Latour, S., Belohradsky, B. H., Leiva, L., Sorensen, R., Debré, M., Casanova, J. L., Blanche, S., Durandy, A., Bushman, F. D., Fischer, A., & Cavazzana-Calvo, M. (2010). Efficacy of gene therapy for X-linked severe combined immunodeficiency. The New England journal of medicine, 363(4), 355–364.
https://doi.org/10.1056/NEJMoa1000164
Kaeppel, C., Beattie, S. G., Fronza, R., van Logtenstein, R., Salmon, F., Schmidt, S., Wolf, S., Nowrouzi, A., Glimm, H., von Kalle, C., Petry, H., Gaudet, D., & Schmidt, M. (2013). Een grotendeels willekeurig AAV-integratieprofiel na LPLD-gentherapie. Nature medicine, 19(7), 889-891.
https://doi.org/10.1038/nm.3230
Masat, E., Pavani, G., & Mingozzi, F. (2013). Humorale immuniteit tegen AAV vectoren in gentherapie: uitdagingen en mogelijke oplossingen. Discovery geneeskunde, 15(85), 379-389.
Mingozzi, F., & Hoog, K. A. (2013). Immuunresponsen op AAV vectoren: het overwinnen van barrières voor succesvolle gentherapie. Bloed, 122(1), 23-36.
https://doi.org/10.1182/blood-2013-01-306647
Joshi, P., Cervera, L., Ahmed, I., Kondratov, O., Zolotukhin, S., Schrag, J., Chahal, P. S., & Kamen, A. A. (2019). Achieving High-Yield Production of Functional AAV5 Gene Delivery Vectors via Fedbatch in an Insect Cell-One Baculovirus System. Molecular therapy. Methoden & klinische ontwikkeling, 13, 279-289.
https://doi.org/10.1016/j.omtm.2019.02.003